Wie Krankheiten entstehen – Ursachenforschung
-
Marine Modellorganismen Nesseltiere oder auch Schwämme gehören zu den ältesten Lebensformen. Sie bevölkern die Ozeane seit Hunderten von Millionen Jahren. Trotz ihres einfachen Aufbaus enthält ihr Erbgut erstaunlich viele Gene. Diese steuern Stoffwechselprozesse, die höhere Lebewesen im Laufe der Evolution zum Teil verloren haben. Nesseltiere oder Schwämme sind damit eine Art Urtyp aller Tiere, an dem sich Grundlagen hervorragend erforschen lassen.
Wie schützt sich ein Organismus vor Krankheitserregern?
Beim Menschen, bei Wirbeltieren und auch wirbellosen Organismen wie den Schwämmen ist die angeborene Immunität eine erste Verteidigungslinie gegen potenzielle Krankheitserreger. Schon Säuglinge verfügen über diesen Schutz, obwohl ihr Immunsystem noch kaum Krankheitserreger kennengelernt hat. Zu diesem stammesgeschichtlich alten Abwehrmechanismus zählen Fresszellen, die Keime vertilgen (Phagozytose), Stoffwechselprozesse, die fremde Eiweiße angreifen und auflösen, oder die Produktion antimikrobieller Peptide. Diese Peptide, die in Tieren, Pflanzen oder auch Mikroorganismen vorkommen, werden von bestimmten Körpergeweben, zum Beispiel Darm, Haut und Lunge, produziert und bilden einen prophylaktischen Schutz gegen Infektionen. Die Immunabwehr des Menschen ist also zumindest zu einem Teil uralt und mit der niederer Organismen verwandt. Zu diesen Lebewesen gehören Schwämme, aber auch Nesseltiere (Korallen, Quallen, Seeanemonen und Süßwasserpolypen), die seit Hunderten von Millionen Jahren im Meer leben und im ständigen Kontakt mit Bakterien und Viren stehen. Es ist daher durchaus möglich, dass die Forscher von ihnen lernen können, wie ein effizientes Abwehrsystem entsteht oder wie man es im Krankheitsfall repariert.
- Nesseltiere (Cnidaria) scheinen besonders geeignet zu sein, um zu klären, wie ein Organismus Bakterien und andere Krankheitserreger in Schach hält, denn sie sind die wohl ursprünglichsten Meeresbewohner. Die Cnidaria sind relativ einfache Organismen, dennoch laufen in und zwischen ihren Körperzellen zahlreiche komplexe Stoffwechselprozesse ab. Auf den ersten Blick scheinen die Nesseltiere leicht verwundbar und wehrlos gegen Krankheitserreger zu sein, denn ihnen fehlt es an Immunzellen, die fremde Keime wegfressen, und an einem Lymphsystem, das Abwehrzellen durch den Körper transportiert. Außerdem haben sie keine feste Schutzhülle, sondern nur eine äußere Zellschicht, das Epithel. Trotzdem haben sie Jahrmillionen überlebt. Das macht sie als Untersuchungsobjekt besonders interessant. Wissenschaftler versuchen zu klären, wie das Gewebe der Tiere mit Mikroben interagiert und wie die Stoffwechselprozesse in der Außenhaut Feinde abwehren.
- Inzwischen ist es gelungen, genveränderte Nesseltiere zu züchten, in deren Körper man antibakterielle Abwehrmoleküle sichtbar macht. Damit können die Forscher am lebenden Objekt untersuchen, wo die Abwehrstoffe freigesetzt werden und wo sie zum Einsatz kommen. Es erscheint wunderbar, dass solche schwachen Winzlinge trotz eines fehlenden Immunsystems und der Abwesenheit patrouillierender Immunzellen in einer Umgebung überleben, die vor potenziellen Krankheitserregern geradezu strotzt. Wie man weiß, sind die Oberflächen vieler Meereslebewesen wie etwa der Schwämme permanent von Bakterien besiedelt. Mehr noch: Ein Liter Meerwasser kann bis zu zwei Billionen Bakterien und noch mehr Viren enthalten. Unter diesen Mikroben befinden sich viele potenzielle Krankheitserreger. Dennoch überleben die Meerestiere. Ursprüngliche Meeresorganismen sind daher attraktive Modellsysteme, um das Zusammenwirken von Körper und Umwelt zu verstehen und die evolutionären Grundlagen zu erforschen. Dank neuer Analysemöglichkeiten nehmen gerade Cnidaria eine reizvolle Rolle bei dem Versuch ein, Einblick in die Evolution von Immunreaktionen zu bekommen, die beteiligten Gene zu identifizieren und die Mechanismen der Interaktion zwischen Tier und Mikroorganismen aufzuklären.
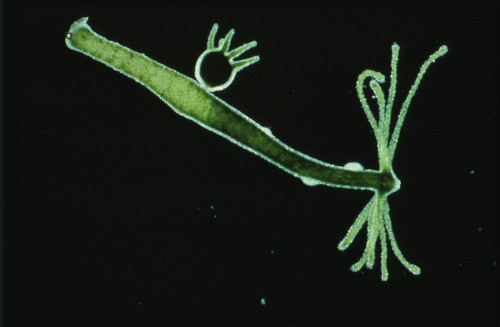
- 9.11 > Seeanemonen gehören zu der artenreichen Gruppe der Nesseltiere, der Cnidaria. Zu ihren Verwandten zählen Korallen und Quallen.

Der Körper und seine Bakterien – ein fein abgestimmtes Miteinander
Höhere Lebewesen und Bakterien stehen in ständigem Kontakt miteinander. Zum einen wirken Bakterien als Krankheitserreger, zum anderen fungieren sie als Symbionten, die zum Teil lebenswichtige Funktionen übernehmen. Der Darm beispielsweise wird von einer komplizierten und dynamischen Gemeinschaft von Mikroorganismen besiedelt, die eine ganze Reihe von Stoffwechselfunktionen unterstützt. Er wird von der Geburt an nach und nach von Bakterien besiedelt. Diese Kolonisierung setzt sich bis in die frühen Lebensphasen fort, bis sich schließlich eine Darmflora gebildet hat, die für jedes Individuum spezifisch ist. Wie das Darmepithel, die äußere Zellschicht im Darm, mit den Mikroorganismen interagiert, wie der Körper zwischen nützlichen Bakterien und potenziellen Krankheitserregern unterscheidet und welchen Einfluss die Bakterien auf die Stoffwechselvorgänge und Leistungsfähigkeit des menschlichen Darmepithels haben, ist weitgehend ungeklärt. Möglicherweise können hier Untersuchungen an Cnidaria weiterhelfen. Auch deren Epithel, die Körperoberfläche, wird von einer komplexen und dynamischen Mikroorganismen-Gemeinschaft kolonisiert. Untersuchungen am Süßwasserpolypen Hydra haben gezeigt, dass sich die Individuen verschiedener Hydra-Spezies beträchtlich in der Zusammensetzung ihrer Mikrofauna unterscheiden.
- Andererseits haben Individuen, die für viele Jahre unter kontrollierten Laborbedingungen gehalten werden, und Individuen derselben Spezies, die man frisch aus ihrem natürlichen Lebensraum gefischt hat, sehr ähnliche bakterielle Zusammensetzungen. Das bedeutet, dass die kolonisierenden Bakterien den Hydra-Individuen lange treu sind. Sie sind permanente Bewohner des Epithels. Die Ergebnisse legen nahe, dass starke Selektionszwänge auf das Epithel wirken. Offenbar etablieren sich unter bestimmten Lebensbedingungen bestimmte Bakteriengemeinschaften auf den Epithelien, die für den Lebensraum optimal sind und lange Zeit konstant bleiben. Diese Beobachtungen legen ferner nahe, dass das Epithel aktiv die Zusammensetzung der mikrobiellen Gemeinschaft formt.
- Entfernt man bei Säugetieren oder Wirbellosen den Bakterienaufwuchs, werden sie in der Regel krank. Der Stoffwechsel wird gestört und das Immunsystem entwickelt sich nur schlecht. Besonders stark sind die Störungen im Verdauungstrakt. Zudem können sich die Tiere kaum mehr gegen Infektionen durch krank machende Bakterien und Viren wehren. Bekannt ist auch, dass bestimmte genetische Defekte im Immunsystem des Menschen das Zusammenwirken des Epithels mit seinen kolonisierenden Mikroben stören können. Betroffene sind meist anfällig für entzündliche Erkrankungen der Barriereorgane wie der Haut oder der Lunge, die eine Grenzfläche zur Außenwelt sind. Obwohl man keine eindeutigen immunbiologischen Erklärungen für die Wirkung der Mikroben hat, ist klar, dass symbiotische Bakterien aktiv an der Balance zwischen Gesundheit und Krankheit beteiligt sind.
- Bakterien sind für viele Organismen also essenziell. Der Tintenfisch Euprymna scolopes zum Beispiel entwickelt während seines Wachstums auf der Hautoberfläche Lichtorgane für Biolumineszenz. Wie ein Glühwürmchen ist der Tintenfisch also in der Lage, durch eine biochemische Reaktion Lichtpulse zu erzeugen. Die Lichtorgane können aber nur dann wachsen, wenn das Epithel des Tintenfischs von dem Bakterium Vibrio fischeri bewohnt wird, das zur Entwicklung des Lichtorgans einen bestimmten Bestandteil aus seiner Bakterienwand beisteuert. Ganz offensichtlich wird bei Wirbeltieren und Wirbellosen also sowohl die körperliche Entwicklung als auch das Immunsystem erheblich von den kolonisierenden Mikroorganismen beeinflusst. Der Einfluss der Bakterien auf die Immunfunktionen und die Mechanismen, die die komplexen Interaktionen zwischen den mikrobiellen Gemeinschaften und den Tieren regulieren, sind bislang aber kaum verstanden. Ungeklärt ist auch, wie der Stoffwechsel im Epithel die Zusammensetzung der symbiontischen Bakteriengemeinschaft beeinflusst. In ersten Experimenten am Polypen Hydra konnte man zeigen, dass Veränderungen an den Zellen die Bakterienflora tatsächlich deutlich verändern. Entfernte man aus dem Gewebe einen bestimmten Zelltyp, änderte sich die bakterielle Zusammensetzung auf der Hydra-Oberfläche deutlich. Die Zahl der normalerweise vorherrschenden Proteobacteria nahm deutlich ab. Die eher selten vorkommenden Bakterien vom Typ Bacteroidetes vermehrten sich hingegen stark. Offensichtlich gibt es tatsächlich eine direkte Interaktion zwischen dem Wirtsepithel und den Mikroben
Krankheiten des Menschen neu verstehen
Viele moderne Krankheiten des Menschen entstehen durch Störungen der Barriere zwischen Körper und Außenwelt. Hierzu gehören chronisch-entzündliche Erkrankungen der Barriereorgane, also von Organen, die im Kontakt mit der Außenwelt stehen – der Haut, der Lunge oder dem Darm, der mit Speisen von außen gefüttert wird. Beispiele sind das Asthma bronchiale (Lunge), die Schuppenflechte und die Neurodermitis (Haut) sowie die chronisch-entzündlichen Darmerkrankungen, der Morbus Crohn und Colitis ulcerosa (Darm). Bei Tieren sind diese Krankheiten interessanterweise gänzlich unbekannt. Systematische genetische Untersuchungen haben gezeigt, dass viele solcher Erkrankungen durch sogenannte Risikogene ausgelöst werden, die evolutionär uralt sind. Das ist paradox, da derartige Erkrankungen erst in den vergangenen Jahren vor allem in den westlichen Industrienationen stark angestiegen sind. Allen Krankheiten ist gemein, dass das Immunsystem des Menschen an den Grenzflächen zur Umwelt aus dem Ruder läuft und körpereigene Strukturen angreift. Neuere Technologien haben es ermöglicht, einzelne gestörte Elemente auf der molekularen Landkarte der Erkrankungen aufzuzeichnen. Diese Einzelbausteine müssen jetzt zu einem Gesamtmodell zusammengesetzt werden, um die Mechanismen zu verstehen, die zu einem fehlgesteuerten Immunsystem führen.
- Aktuelle Forschungsergebnisse deuten darauf hin, dass an der Fehlsteuerung des Immunsystems viele Gene beteiligt sind, die die entwicklungsgeschichtlich alten Formen der immunologischen Auseinandersetzung mit der Umwelt, wie zum Beispiel mit der umgebenden mikrobiellen Flora, steuern.
Eine Frage ist, wie im Laufe der Evolution genetische Variabilität in jenen Genen entstehen konnte, die die Eigenschaften der Barriere bestimmen. Wie verändern schwankende Nahrungsbedingungen oder eine andere Mikroflora im Wasser die genetische Variabilität der Barriere? Wie beeinflussen solche Veränderungen die evolutionäre Fitness von Organismen, also die Wahrscheinlichkeit, dass sich seine Gene in der Evolution durchsetzen? Versteht man die Vorgänge auf der Oberfläche der Meerestiere, so kann man künftig möglicherweise besser nachvollziehen, wie Erkrankungen der Barriereorgane beim Menschen entstehen. Hat man erst einmal die Evolution und Funktion der Barrieregene enträtselt, lassen sich vielleicht sogar neue Strategien zur Behandlung dieser Krankheiten oder zur Prävention finden. In den vergangenen Jahrzehnten hat man an ausgewählten Modellorganismen wie der Maus oder der Fruchtfliege Drosophila melanogaster viel darüber gelernt, wie die Auslöser von Krankheiten erkannt und bekämpft werden. Warum die Außenhaut eines jeden Organismus von Mikroben besiedelt wird und wie diese Mikroben mit dem Wirt interagieren, weiß man bis heute aber nicht.